分级枝状铜基材料及电催化性能研究毕业论文
2020-02-19 16:02:12
摘 要
本文通过金属置换法和电化学沉积法制备了铜-氧化亚铜、铜-氧化亚铜-钌、铜-氧化亚铜-银三种体系的具有分级枝状结构的铜基材料。通过改变沉积电流大小和沉积时间有效的调控了其结构从球状颗粒到分级枝状结构的转化,并且使用电化学工作站测试了三种材料的电解水析氧催化性能。论文主要研究了铜基材料的形貌结构对电催化性能的影响以及其他金属的引入对电催化性能的影响。研究结果表明:分级枝状结构的铜基材料相比球状颗粒结构的铜基材料电解水析氧性能(OER)更好。
本文的特色:采用简单的金属置换法制备了铜-氧化亚铜-银复合材料,利用电沉积法制备出分级枝状结构的铜-氧化亚铜体系材料,并测试了其电解水催化性能。
关键词:分级枝状结构,铜基材料,电沉积,电催化
Abstract
In this paper, Cu-Cu2O, Cu-Cu2O-Ru and Cu-Cu2O-Ag with hierarchically dendritic structure were prepared by metal replacement reaction and electrochemical deposition. The transformation from spherical-like nanoparticle to hierarchically dendritic structure was effectively regulated by changing the deposition current and deposition time, and electrocatalytic oxygen evolution performance of the three materials were tested by using an electrochemical workstation. The influence of the morphology and structure of copper based materials on the electrocatalytic performance and the influence of the other metals on the electrocatalytic performance were studied. The results show that copper based materials with hierarchically dendritic structure have better electrocatalytic oxygen evolution performance than spherical copper based materials. Characteristics of this work: Cu-Cu2O-Ag was prepared by metal replacement reaction, copper-cuprous oxide system material with hierarchically dendritic structure was prepared by electrodeposition method, and its electrocatalytic water oxidation performance was tested.
Key Words:Hierarchically dendritic Structure, Copper-based materials, Electrodeposition, Electrocatalysis
目录
第一章 绪论 1
1.1 分级枝状材料概述 1
1.2 分级枝状材料制备方法概述 1
1.3 铜基材料在电催化中的应用 6
1.4 本论文的设计思路和研究内容 11
第二章 分级枝状Cu-Cu2O材料及电催化析氧性能研究 12
2.1 实验药品及仪器 12
2.2 材料的物理性能表征 13
2.3 材料的电解水性能测试 13
2.4 分级枝状Cu-Cu2O材料的制备 15
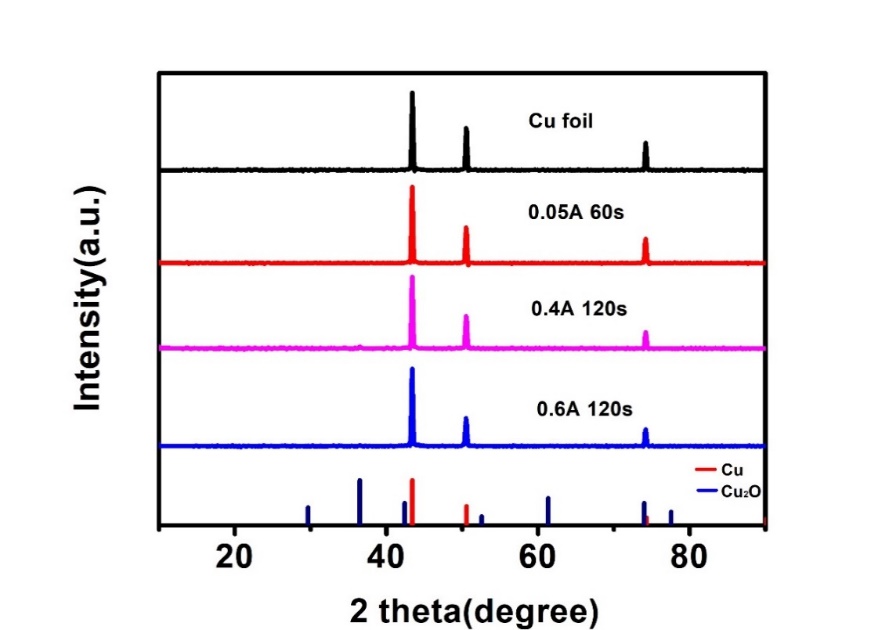
2.5 形貌调控与物相表征 15
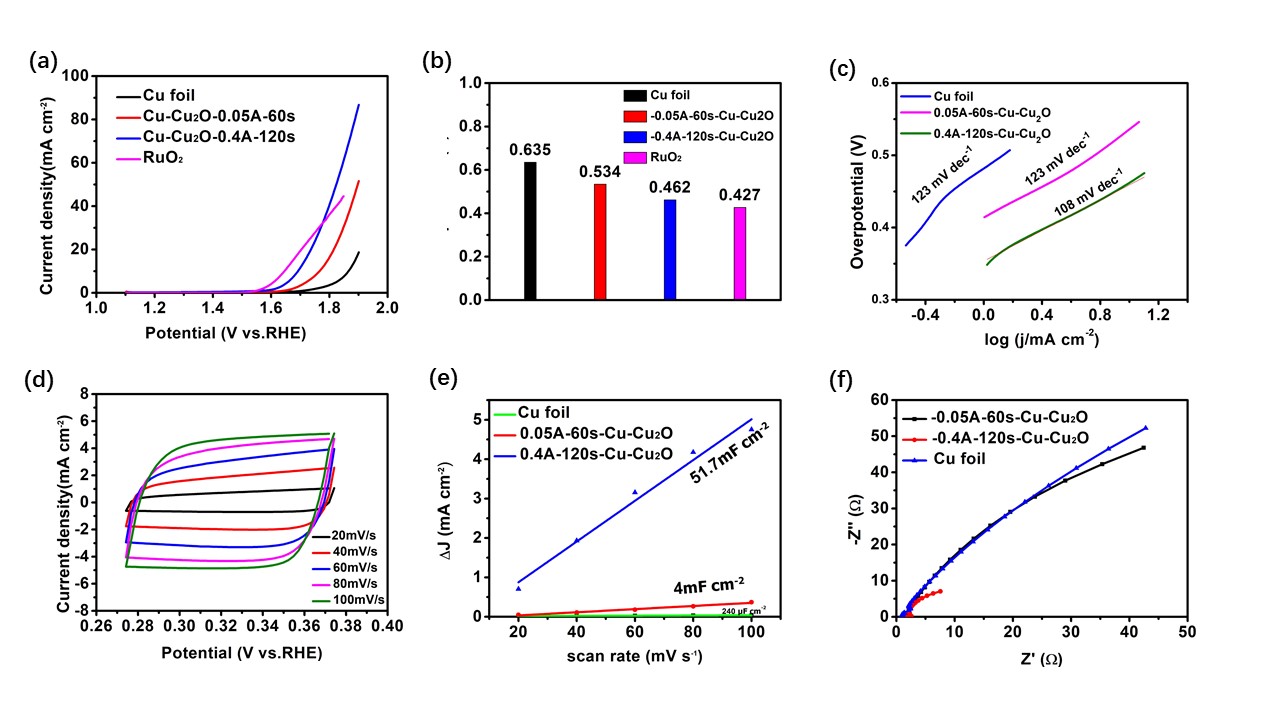
2.6 电解水性能 19
第三章 分级枝状铜基金属复合材料及电催化性能研究 21
3.1 分级枝状Cu-Cu2O-Ag、Cu-Cu2O-Ru的制备 21
3.2 形貌与物相表征 21
3.3 电解水性能 24
第四章 结论与展望 25
4.1 结论 25
4.2 展望 25
参考文献 26
致谢 28
第1章 绪论
1.1分级枝状材料概述
金属纳米晶体因为其独特的结构、物理化学性质,在催化剂、传感器和纳米器件等方面具有巨大应用潜力,已经成为材料领域的研究热点。随着研究的深入,人们发现金属纳米晶体材料表现出来的催化活性、敏感度等性能与其结构有着密不可分的关系,因此,控制金属纳米晶体的形貌对现代材料化学至关重要,它的物理和化学性质可以通过简单调节材料的尺寸和形状而得到调控。优良的合成性能和加工性能使得金属纳米晶体在成像、电子、催化、传感、光子学和医学等领域具有十分广阔的应用前景。而在这些应用中,金属纳米晶体的形状控制不仅对其性能的最大化至关重要,而且对充分开发这些具有优越性能的纳米材料的潜力也至关重要。
金属纳米晶体具有多种多样的结构:球状结构、片状结构、枝状结构等等。球状结构主要分为“棒球”和“片球”两种:“棒球”结构是由一维纳米线或纳米棒组装而成的;“片球”结构则是由多片纳米片拼装而成;片状结构则表现为尺寸相近且均匀分布的纳米片;枝状晶体则是像自然界中的树枝一样,具有一级、二级和高度有序的分级结构[1-5]。
近年来,枝状晶体结构因其具备高度有序的分级结构而受到越来越多的关注。枝状晶体的形成主要是由于其生长界面的稳定性造成破坏,这是一种非平衡的过程。在1974年,Ivantsov提出了枝状晶体形成的扩散传输理论,成为了后来研究枝晶形成理论的基础[6]。在这一理论体系中,宏观动力学因素(扩散场、热力学、表面活性剂等)被研究者们认为是起到主要作用,然而,微观动力学因素(表面张力、表面动力等)的作用却为他们所忽视。对枝晶形成研究的不断深入使得研究者们发现:微观动力学因素同样会对枝晶的形成起着重要作用,有时甚至是决定性作用。

图1.1 a是Cu枝晶结构的SEM图;b, c为其高倍SEM图
1.2分级枝状材料的制备方法
近些年,许多具有枝状形貌的金属纳米晶体,如多枝晶和纳米枝晶的液相合成方法得到了发展,其主要的合成方法有:水热法、金属置换法、电沉积法等。
1.2.1水热法
水热法是指:在密封的压力容器中,以水作为溶剂、药品粉体经溶解和再结晶的制备材料的方法。相较于其他制备方法,水热法制备的材料有着晶粒发育完整,分布均匀,粒度小,颗粒团聚较轻,可使用较为便宜的原料,易得到合适的化学计量物和晶形等优点。Yang Yang, Shao-Yun Fu等人将氯化钴水溶液在110℃下反应60分钟,生成了金属单质钴的枝状晶体[7];Hai-Ping Qi, Nan Tao等人将二氧化镍和次磷酸的水溶液在160℃反应24小时后,得到了微米级镍树枝状晶体[8];而Zhiping Yang, Yitai Qian等人则是在室温下,在乙醇中与水合肼还原Co2 ,合成了树枝状钴纳米晶[9]。
1.2.2金属置换法
一般情况下,置换反应可分为两种:(1)固体与固体之间在高温或加热条件下发生置换反应;(2)固体在水溶液中进行液态置换。制备枝状晶体的置换法一般为液态置换,即在金属盐溶液中加入金属单质来置换出所需金属。金属置换反应所需反应时间不长且反应温度也较低,一般为室温或40℃到80℃之间,实验操作简单,形成的枝状晶体结构较均匀,常为多枝状,枝较短。Yan Fang等人将铜箔放入硝酸银溶液中进行置换,成功合成了铜银枝状结构合金[10];Zhimao Yang等人将锌箔置入HCuCl2溶液中制备出形如稻谷的铜锌枝状结构晶体[11];Bingjun Ding等人在硝酸银溶液中加入锌箔,制备出银枝晶[12]。
1.2.3电沉积法
电化学沉积法是采用三电极电池进行沉积,用碳纸、金属箔或泡沫镍网作工作电极采用铂丝电极作为对电极、Ag/AgCl电极为参比电极,通过调节电压、电流和时间在其表面沉积出所需金属。电化学沉积法较水热法和金属置换法而言,反应通常在常温下进行,反应速度更快,一般为几十秒或几分钟,且能通过改变电流电压和沉积时间等参数对合成的材料结构进行有选择性的调控。电沉积法制备的材料结构非常均匀,但是可能因为沉积电位过高或沉积电流过大而生成副产物。Zhiyu Hu等人以铂网为衬底,在物质的量浓度为2 mM的K2PtCl6 和0.5 M H2SO4水溶液中沉积Pt,设置上电位EU=0.4 V, 0.5 V, 0.6 V, 1V ,下电位EL= -0.25 V,脉冲电位频率f = 10 Hz,沉积时间t =400 s,实现了颗粒形态从半球、纳米颗粒向纳米枝晶的转变[13]。Qixian Zhang和Li Niu等人采用一种简单方便的电化学方法——差脉冲安培法来控制电沉积反应,不同于一般的恒电位或循环电位的电沉积,差脉冲安培法利用脉冲电位作为沉积和溶解电位。他们以ITO载玻片为沉底,在0.5 M H2SO4 和2 mM 的四氯丙二酸钠 (Na2PdCl4)溶液中经氮气鼓泡脱气20 min后进行电沉积,以-0.2 V 到1.2 V为EL和EU的不同脉冲电位,在10 Hz下,以DPA模式电沉积Pd纳米粒子,循环12000次,成功地在导电衬底上沉积了树枝状、仙人掌状、片状和针刺状等结构的Pd晶体[14]。
1.3铜基材料在电催化中的应用
1.3.1电催化分解水概述
石油、煤炭等不可再生能源的过度使用给全球经济的发展造成了严重的影响,空气污染问题亟待解决,全球气候变暖愈演愈烈,环境问题成为了人们不得不面对的问题,随着化石类不可再生能源的日渐枯竭,寻找一种清洁无污染可再生的新型能源来替代化石类不可再生能源就成为了解决环境问题的关键。在众多的新型能源中,构建以氢能为核心的能源体系成为一项十分可行的方案。
氢能是21世纪最有前景的能源之一,其主要优势在于:清洁无污染、燃烧热值高、资源较丰富、适用范围广泛等。浩瀚的大海中蕴含着丰富的氢,若能够将其全部提炼出来,大约可以达到1.4×1017 t,所能产生的热量约为地球上所有矿物燃料的9000倍。实现氢能广泛应用的关键技术有两个:一方面要能够大量制取氢气;一方面要解决储氢和运输氢的问题。而其中最重要的就是氢的制取问题。
制氢的方法主要有电解水制氢、生物质制氢、光解水制氢、矿物质制氢、利用化工过程的副产物制备氢气等。目前,工业化产氢的方法主要分为三类:蒸汽甲烷重整法、煤气化法和电解水法。在这些方法中,蒸汽甲烷重整法和煤气化法的产量约占氢气总产量的95%以上,而电解水法只占氢气总产量的4%左右。显然,目前的工业化制氢还严重依赖化石类不可再生能源,而这些方法并不能解决日益严重的二氧化碳排放和环境污染等问题。蒸汽甲烷重整法是依靠高温下,碳氢化合物与水反应而析出氢气,这一过程不单单产生了氢气,还生成了大量的二氧化碳,而这些二氧化碳如果被排放到大气中,势必会加剧本已严重的温室效应。由此可见,蒸汽甲烷重整法对环境改善的作用不大,甚至还加剧了环境污染和气候变暖。煤气化法仍无法避开对化石类能源的依赖,不能成为现在亟待解决的环境污染和气候变暖问题的对策。而在这三种方法中,电解水在对不可再生能源的依赖性和其简单的反应过程等方面上更具发展前景。
电解水的研究已经有相当一段时间,但碍于成本和其他因素的影响,电解水制氢一直无法在工业上大规模应用,但全球众多的研究者依然希望能够通过技术进步以及物质创新来大幅度降低电解水的成本,来将其推向大规模工业化的应用。典型的电催化析氢反应体系由三部分构成:阴极、阳极和电解质。阳极上含有氧反应催化剂(OEC),阴极上含有氢反应催化剂(HEC)来促进水的分解反应,当外界有电压作为驱动时,水分子可以分解成氢气和氧气。根据电解液的不同,电极上的反应过程也不同,其反应式如下:
总反应: H2O→H2 1/2O2
在酸性介质中:
阴极: 2H 2e-→H2
阳极: H2O→2H 1/2O2 2e-
在碱性介质和中性介质中:
阴极: 2H2O 2e-→H2 2OH-
阳极: 2OH-→H2O 1/2O2 2e-
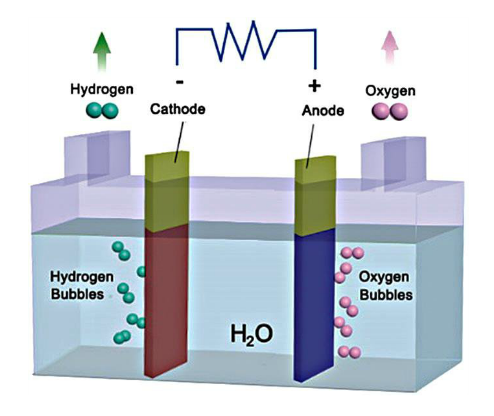
图1.2 电解槽原理图
在一个大气压下,无论处于何种电介质中,水分解的热力学电压都应该是1.23 V, 这个热力学电压主要与温度有关,热力学电压随温度的升高而降低。而实际操作中,电极电压会高于理论的电极电压,这部分高出的量被称为过电位,用η表示。过电位主要用于克服反应阴极和阳极上的内在活化阻力,阴极过电位和阳极过电位分别以ηa和ηb表示,除此之外还有类如溶液阻力、接触阻力等因素,我们用ηother来表示。所以,实际操作中水的电解电压(EOP)应为:
EOP=1.23V ηa ηb ηother
过高的电解电压会造成能量的损耗,同时,倘若电极电压过高,电极上很容易发生一些副反应,这将会严重影响电极和催化剂寿命并且造成能量的损耗。由上述等式我们可以看出,若想降低水的电解电压,最关键的就是要降低反应中的过电位,使得电解水的能耗降低。等式中的ηother可以通过改进电解池来降低,而ηa和ηb则可以通过采用高效的阴极和阳极电催化剂来降低。Tafel在研究归纳了大量的析氢反应动力学数据之后,总结了过电位和电流密度之间的关系式,也就是著名的Tafel公式。在金属表面发生的析氢反应有如下关系:
η=a blgi
其中,a和b为常数,单位是V,a的含义是在电流密度i为1 A/cm2时的过电位值,它的大小和电极材料的性质、电极表面状态、溶液组成及温度等因素有关,根据a值的大小,可以比较不同电极体系中进行电子转移步骤的难易程度。对于大多数金属,b是一个与温度具有主要关联的常数,常温下b的数值在0.12 V左右。η为过电位,i为电流密度。这一总结出的经验公式目前仍是研究电化学动力学的重要工具。
长期的研究发现,在电解水过程中效率最高的析氢(HER)和析氧(OER)催化剂是以Pt, Ru, Ir等为代表的贵金属,这些贵金属的高昂价格以及在地球上稀少储量成为了导致电解水高成本的主要因素,也是掣肘大规模工业化产氢的重要原因。在此背景下,为了使电解水制氢的过程更加经济,最理想的方案就是使用一种在地球上储量大,并且具有良好导电性的元素来开发出高效的电催化剂,从而提高电解水制氢过程的能效。
1.3.2铜基材料在电解水中的应用
以Pt, Ru, Ir等为代表的贵金属催化剂虽然具备优良的催化性能,但是由于价格昂贵,储量较少,导致其无法进入工业化大规模应用。因此,研究者们进行了大量的研究以开发高效的非贵金属催化剂,如过渡金属氧化物、硫化物、磷化物等。
铜是一种具有优良导电性的金属,其导电性在所有金属中仅次于银,不过铜元素在地球上储量较大,这使它成本低廉,这种独特的优势使其在电极材料领域具有光明的发展前景。近年来,铜基合金、铜氧化物和铜磷化物等展现出不错的电化学性能,而在电解水中,铜基材料一般用于析氧反应(OER) Lin Guo团队采用快速光腐蚀方法合成了均匀非晶纳米铜镍铁氧化物,在碱性溶液中OER的Tafel 斜率为44 mV dec-1,该催化剂在过电位300 mV时表现出非常大的质量活性,为1464.5 Ag-1 ,为已知的最高质量活性,这一合成策略为制备铜基三元非晶纳米材料提供一条全新的途径[15];Yilin Deng课题组采用原位拉曼光谱分析技术,研究比较了Cu, Cu2O, CuO和Cu(OH)2这几种铜基催化剂的析氧反应(OER)过程,指出在OER反应过程中,作为催化活性中心的是CuⅢ氧化物,为研究铜基电催化剂的OER反应过程提供了指导[16]。
1.3.3电催化CO2还原概述
化石类不可再生能源的大量使用不仅带来了严重的能源危机,也使得大气中的CO2含量急剧上升加重温室效应,一种两全其美的解决方法就是将大气中的CO2转化为能被人们利用的碳氢化合物从而降低大气中的碳含量以及生成具有附加值的产品。自1960年代到今天,人们一直在研究通过化学合成的催化剂与人工搭建的光电化学体系来模拟自然界进行人工光合作用的可能,即人工光合作用。在众多人工光合作用的体系中,太阳能驱动的电催化还原CO2因为更高效且实用而被广泛研究。在电催化还原CO2的过程中,除主要产物外,由于副产物的多样性,使得在保证高效催化生成产物的同时还保持高的选择性成为了一项重大的挑战。
CO2电催化还原的机理比较复杂,依据产物的不同可分为两电子、四电子、六电子以及八电子过程。并且从动力学上讲,即便是在具有较高活性的催化剂表面,这些反应速率都相当缓慢。目前已知的高选择性催化剂多为金属催化剂,并可依据其主要产物的不同分为三类:(1)产物以甲酸或甲酸盐为主的Sn, Pb和Bi等金属对CO2中间体的吸附能力较弱的金属催化剂;(2)对*COOH有较强吸附但对*CO吸附较弱,主要产物为CO的金属材料,如Au, Ag, Pb和Zn等;(3)能够将CO进一步还原为如碳氢化合物和醇类等重要工业原料的金属催化剂,而Cu为目前己知的唯一材料,这是其它金属催化剂所不能替代的。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: